(1)MnO2+4HCl=MnCl2+Cl2↑+2H2O(2)2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+8H2O(3)Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O这三个式子中哪个不是生成1molCl2时转移2mol电子,为什么
来源:学生作业帮助网 编辑:作业帮 时间:2024/04/24 10:24:17
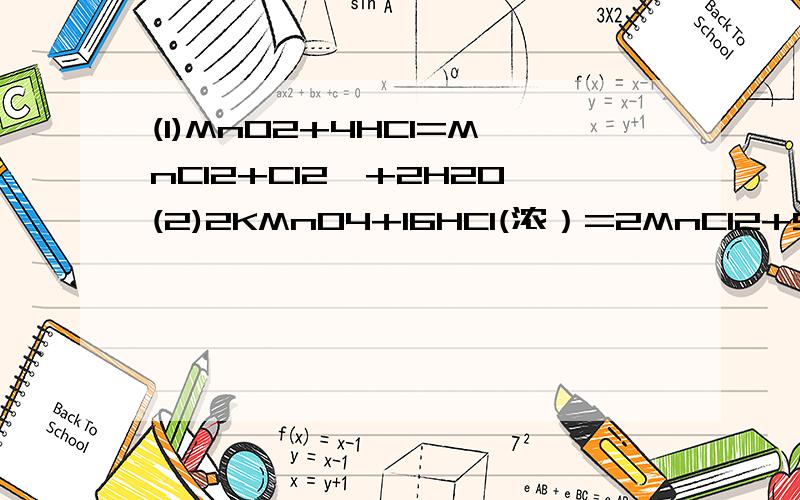
(1)MnO2+4HCl=MnCl2+Cl2↑+2H2O(2)2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+8H2O(3)Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O这三个式子中哪个不是生成1molCl2时转移2mol电子,为什么
(1)MnO2+4HCl=MnCl2+Cl2↑+2H2O
(2)2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+8H2O
(3)Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
这三个式子中哪个不是生成1molCl2时转移2mol电子,为什么
(1)MnO2+4HCl=MnCl2+Cl2↑+2H2O(2)2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+8H2O(3)Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O这三个式子中哪个不是生成1molCl2时转移2mol电子,为什么
(2)2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+8H2O
这条题目错了吧前面16个Cl,后面只有14个Cl
个人感觉是3错Ca(ClO)2中Cl是+1价,HCl是-1价.2个Cl+1转换为Cl2,2个Cl-1转换为Cl2
只转移了一mol
选3,12都是2个Cl-失去2个电子,生成1mol Cl2
3是1个ClO-和1个Cl-结合生成1mol Cl2,Cl-失去1个电子,ClO-得到1个电子,转移1mol电子
第三个,从反应前后Cl离子的化合价可以判断。产物中的每1mol的Cl2是次氯酸钙提供1mol的Cl以及浓盐酸提供的1mol的Cl生成的,其中次氯酸钙中的Cl呈+1价,盐酸中的Cl呈-1价,只转移了1mol的电子。